Inhalt
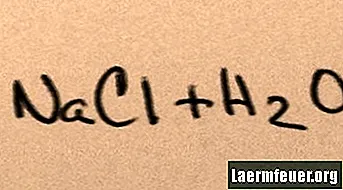
Wenn Salz zu Wasser gegeben wird, löst es sich in seinen Molekülkomponenten auf, bis die maximalen Salzionen, die das Wasser unterstützen kann, um die Wasserstoff- und Sauerstoffmoleküle schweben. In diesem Fall wird die Lösung als "gesättigt" bezeichnet. Wenn mehr Salz gelöst wird, kollidieren Natrium- und Chloridionen miteinander und rekombinieren in Salzkristallen. Dieses Phänomen ist als "Niederschlag" bekannt, da der gebildete Feststoff auf den Grund des Wassers fällt. Salze sind "hydrophil", dh sie werden von Wasser angezogen. Diese Anziehungskraft ermöglicht eine bekannte Form des Niederschlags: Regentropfen bilden sich um winzige Salzkristalle in den Wolken und lassen sie leicht salzig schmecken.
Das Grundlegende

Elektrolyte

Salz leitet Elektrizität nicht in festem Zustand, aber in flüssigem (flüssigem) Zustand bildet es eine Lösung, die Elektrizität sehr gut leiten kann. Die Leitfähigkeit hängt von der Art des verwendeten Salzes ab, aber diese Flüssigkeiten, sogenannte Elektrolytlösungen, sind ausgezeichnete Träger von Verbindungen, die vom menschlichen Körper benötigt werden. Die vom Gehirn erzeugten elektrischen Impulse produzieren freien Sauerstoff, der vom Blut genutzt wird. Die Salzmoleküle werden in Elektrolyte (Natrium, Kalium oder Kalzium) und Chloride in Lösung eingeteilt: Das Chlorid wird von Blut und Nieren in den Urin gepumpt, und die Elektrolyte werden in einem von Sportlern als Prozess bezeichneten Prozess über das neuromuskuläre System verteilt Rehydration.
Kolligative Eigenschaften

Jede Lösung unterscheidet sich von ihrer ursprünglichen Zusammensetzung, da die Zugabe von Molekülen, selbst wenn sie keine neuen Verbindungen bilden, das Molekulargewicht der Flüssigkeit verändert und ihre Eigenschaften beeinflusst. Salzwasser ist dichter als reines Wasser und gefriert auch langsamer. Beim Gefrieren wandert das Salz jedoch an die Grenzen der Flüssigkeit, wodurch es schwerer und gesättigter wird und dann seinen Gefrierpunkt senkt. Am anderen Ende des Materiezustands, je dichter das Salzwasser ist, desto mehr Wärme wird benötigt, um zu verdampfen, bis das Wasser ausgeht und eine Salzschicht zurückbleibt. Die Köche warten, bis das Wasser im Topf kocht, um Salz hinzuzufügen, um das Erhitzen nicht zu verzögern. Diese Eigenschaften, die als "kolligative Eigenschaften" bekannt sind, helfen Wissenschaftlern, das Molekulargewicht von Salzwasser zu bestimmen. Wenn die Masse, der atmosphärische Druck und der Siedepunkt der Flüssigkeit gemessen werden können, können Wissenschaftler das Molekulargewicht des Wassers subtrahieren, um herauszufinden, welche Salze vorhanden sind.